2024-12-13 17:23:57 健康 16039阅读
2024年12月12日,三英综合医院、三英研究所(TAMRI)在卫生部、外交部和美国疾病预防控制中心(CDC)代表见证下,宣布实施VISTA-1 项目的 RBS2418 药物。这是一款经美国食品药品监督管理局(FDA)批准进入临床试验的美国口服免疫癌症治疗药物。该药物为口服形式,使用方便,降低了成本,为很多患者增加了获得机会,特别是治疗费用非常高的癌症。

越南三映综合医院是美国以外第一个参与口腔免疫癌症治疗药物临床试验的研究机构。
RBS2418通过将肿瘤的“免疫状态”从“冷”转为“热”的机制,激活人体的免疫系统,识别并消灭癌细胞。该药物在临床前测试中已被证明是安全的在美国10多家知名医院和医学院的1期临床试验项目中,并未对癌症患者造成明显的副作用。这些研究数据表明,RBS2418无论是单独使用还是与免疫检查点抑制剂(抗PD-1)联合使用,都具有对抗肿瘤进展的潜在功效。
凭借一期的良好结果,RBS2418继续被批准用于癌症患者反应有效性的二期研究,首先是晚期结直肠癌,患者对现有的治疗方法不再有反应。预计VISTA-1将在美国和越南招募150名患者。越南在 5 个研究机构部署了该系统,最初是在河内的 Tam Anh 综合医院和胡志明市的 Tam Anh 综合医院,预计在不久的将来扩展到其他 3 个医院。

教授、博士。 Jeffrey S. Glenn强调,该项目使越南患者比其他人早很多年获得药物其他国家的人们
癌症是越南的主要原因之一,每年有超过12万人死于这种疾病。其中,结直肠癌呈明显增加趋势。具体来说,根据国际癌症研究机构(IARC)Globocan项目的预测,到2045年,仅亚洲地区结直肠癌的死亡率就可能比现在增加到近80%。
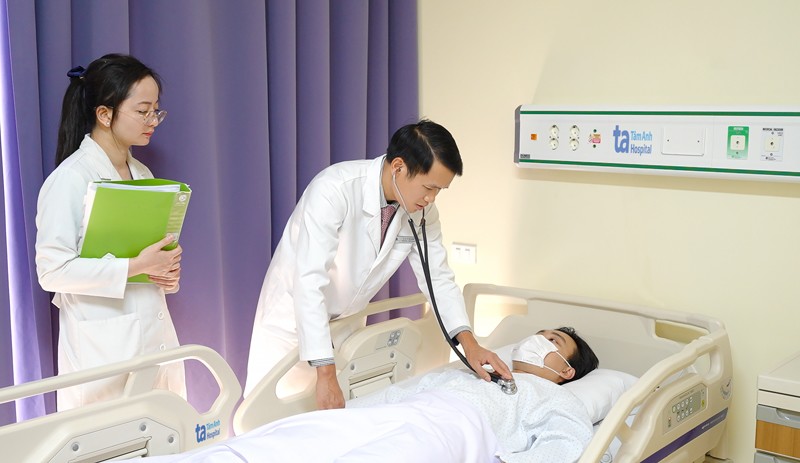
河内三英综合医院肿瘤科主任武友谦医生表示,结直肠癌治疗的一大挑战是发现时已处于晚期,且死亡率低、转移率高。 。这使得治疗过程变得非常困难,转移性结直肠癌患者的5年生存率只有10-20%左右。同时在越南,对于许多转移期的癌症,如果使用靶向药物或免疫药物,5年生存率为30-40%。虽然目前癌症治疗的指南和建议有限i 越南与世界相似,但治疗方法仍然有限,因为疾病严重,发现时已处于晚期,对治疗的反应能力不高。
在此背景下,美国生物技术公司Riboscience的VISTA-1研究——由斯坦福大学医学院杰出医学教授Jeffrey S. Glenn教授等一批著名专家开发; Klaus Klumpp博士,世界著名制药公司分子生物学和创新药物研究员,Riboscience联合创始人兼董事长;斯坦福大学药物化学系主任马克·史密斯博士的目标是在利用免疫机制治疗对当前方法不再有反应的晚期癌症时,努力带来突破性的解决方案。在当前阶段,该研究重点关注治疗失败的转移性进展性结直肠癌患者。或对现有疗法不耐受,从而为他们提供创新和潜在的解决方案。
Tam Anh研究所执行主任Phuong Le Tri博士肯定:“VISTA-1是越南抗击结直肠癌的重要一步。这项研究不仅为患者带来新的机会,也肯定了越南的医学研究能力Tam Anh 综合医院和 TAMRI 参与 VISTA-1 体现了我们对创新应用的承诺。学习最新技术,提高越南人民的医疗保健质量。”
 Phuong Le Tri医生肯定VISTA-1是越南抗击结直肠癌的重要一步
Phuong Le Tri医生肯定VISTA-1是越南抗击结直肠癌的重要一步
过去,越南往往只参加新药3期临床试验。据卫生部科学技术与培训司司长Nguyen Ngo Quang博士介绍,VISTA-1项目的药物RBS2418是越南第一个治疗癌症的2a期临床试验。同时,这也是首次将新的生物标志物检测从一开始就进行技术转移,并将在越南研究中心的中心实验室进行,而无需转移到国外实验室。
教授、博士。 Jeffrey S. Glenn强调,通过这个项目,越南有机会很早就参与药物开发阶段,让患者比其他国家的人早很多年获得药物。 “目前,患者必须来美国参与研究。越南是美国以外患者可以获得这种药物的唯一地方。”他进一步解释道。
VISTA-1不仅为人们提供了早期获得先进癌症治疗方法的机会,也是越南医疗行业和创新突破性科学向前迈出的重要一步。参与VIST等国际临床试验A-1还帮助越南建立了越南人的治疗数据库,为完善药品记录和推动新药在越南流通的许可进程做出了贡献。
| 三映综合医院:cskh@tahospital.vn 三英研究所:vanphong.hcmc@tamri.vn
|